ПАРАДОКСЫ ФИЗИКИ
ПЕРЕПИСКА С ЧИТАТЕЛЯМИ
ЕЩЕ РАЗ ОБ ОПЫТЕ КРАПИВИНА*
* Мы не повторяем описания опыта, ограничиваясь необходимыми цитатами; желающих подробно с ним ознакомиться отсылаем к журналу «Наука и жизнь» № 9 за 1984 г., к статье «Парадоксы физики».
Все авторы писем в редакцию (за исключением одного, просившего не упоминать его фамилию) согласны с тем, что «опыт Крапивина» ни в какой степени не дает оснований сомневаться в правильности второго начала термодинамики.
Читатель, «опровергающий» второе начало термодинамики, исходит из тех же положений, что и другие изобретатели вечного двигателя второго рода: возможности «концентрировать тепло окружающей среды». Поэтому, не вникая в детали «опыта Крапивина», он признал его результат вполне естественным, не усмотрел в нем никаких парадоксов и считает, что «можно нагреть воду до 110'С не только паром, но и теплом окружающей среды».
О неверности такой точки зрения уже много написано в литературе о вечном двигателе.
Остальные письма посвящены в основном природе эффекта, наблюдаемого в «опыте Крапивина». По поводу того, как наиболее правильно объяснить этот эффект, мнения авторов писем разошлись.
Большинство из них, например, семья Волковых (г. Омск), Е. Каштанов (г. Шевченко), И. Леенсон (г. Москва), Н. Лучинский (г. Москва), П. Мищенко (r. Белая Церковь), Ф. Руссу (г. Тирасполь) считают правильным и достаточным объяснение А. В. Шубникова: причина нагрева — теплота конденсации пузырьков пара, и неверным объяснение в комментариях: причина — теплота растворения.
Вот что пишет, например, Е. Каштанов: «Академик Шубников совершенно убедительно и неоспоримо описывает механизм процесса. И чувствуется, что иначе и быть не может — пар, являясь пересыщенным по отношению к раствору, должен конденсироваться, а куда же деваться теплоте конденсации, как не идти на нагрев раствора, хотя его температура и выше, чем у пара. Но как это все согласуется со вторым законом, Шубников подробно не объясняет. Теперь в комментариях к статье нам обещают раскрыть это отношение и более доказательно установить, опровергает «опыт Крапивина» второе начало или нет. Суть объяснения сводится к указанию на теплоту растворения соли «дающей добавочный эффект разогрева». А ведь это совсем неверно! Во-первых, добавочный разогрев не обязателен, достаточно и основного, чтобы температура раствора поднималась. Ведь никто, кажется, не спорит, что пар конденсируется! Но главное в том, что поваренная соль растворяется в воде не с выделением, а с поглощением тепла. Так что источник разогрева один - стоградусный пар».
В комментариях к статье А. В. Шубникова вовсе не утверждается, что добавочный разогрев рассола (то есть нагрев до температуры выше 100'С) связан только с тепловым эффектом растворения соли в воде.
Там сказано: «Здесь происходит не просто нагрев, а смешение пара с соленой водой.
В этом, как уже нетрудно догадаться, «вся соль» вопроса. И далее: «Эти два процесса растворения — пузырьков пара в рассоле и соли в нем — и приводят к нагреванию рассола до температуры, существенно более высокой, чем 100'С».
Таким образом, речь идет о суммарном эффекте двух процессов.
Теплота растворения пара в насыщенном рассоле приводит к его нагреву. Поскольку она существенно больше, чем теплота растворения соли в жидкой воде (это приводит к охлаждению рассола, вернее, уменьшению его нагрева), то естественно, что доминирует первый эффект.
Важное значение второго эффекта, несмотря на то, что он эндотермический - идет с поглощением тепла — и относительно небольшой, состоит в подпитке раствора солью. Если раствор не будет насыщенным, то эффект дополнительного разогрева хотя и будет, но уменьшится и максимальная температура рассола не достигнет 110'С. Все эти положения никоим образом не означают отрицания общеизвестного факта охлаждения воды при растворении в ней поваренной соли.
Повод к такого рода трактовке дала' фраза комментария: «Можно сказать, что соль, смешиваясь с водой, «отдает свой долг» — то тепло, которое было затрачено на ее отделение от воды при добыче из раствора». Действительно, сказано неудачно.
Нужно было пояснить, что речь идет об отделении соли от воды классическим методом: с помощью испарения раствора. (Автору комментария не следовало забывать полезный афоризм: «Попытки чрезмерно упростить приводят к сложностям».) О какой же «отдаче долга» все-таки идет речь| Разберем это положение по существу. Для этого поставим «опыт Крапивина» в несколько ином варианте, который позволяет вести процесс в обоих направлениях: с растворением пара в рассоле и соли в воде, и в обратном — с выделением пара и выпадением соли. Представим себе сосуд со свободно движущимся невесомым поршнем, который отделяет его внутреннюю полость от атмосферы. В сосуда находятся в равновесии насыщенный раствор соли, водяной пар над ним и кристаллическая соль — на дне. Предположим, что сосуд предварительно был нагрет до 100'С и в него, как в «опыте Крапивина», подается через трубку водяной пар с температурой тоже 100'С (рис. 1). Пар растворяется в жидкости, и температура рассола, как мы уже знаем, постепенно повышается до 110'С, а соль при этом растворяется в воде. Свободный поршень поддерживает давление в сосуде равным атмосферному, независимо от количества пара.
Процесс можно продолжить и тогда, когда будет достигнута температура 110'С.
Теперь, чтобы соль и пар продолжали растворяться, нужно отводить от сосуда тепло (рис. 1), в количестве, равном, как уже отмечалось, разности между выделяющимся при взаимодействии пара и рассола и поглощающимся при растворении соли в воде.
В условиях термодинамического равновесия процесс может продолжаться при той же температура рассола 110'С до тех пор, пока на дне хватит соли для подпитки увеличивающегося количества рассола. Как только вся соль растворится, температура рассола начнет снижаться, хотя и останется выше 100'С. В пределе, как и сказано в комментарии, она стремится к 100 С, но это, разумеется, можно представить лишь теоретически, при бесконечном разбавлении раствора.
Пусть теперь процесс идет в обратном направлении: будем не отводить тепло от рассола, а подводить к нему; при этом надо, конечно, повернуть трубку отверстием вверх, чтобы пар мог выходить наружу (рис. 2). Тогда концентрация соли в растворе будет расти, а затем, при температуре 110'С, соль начнет выпадать на дно.
Подчеркнем, что непременным условием такого выделения служит подвод тепла, так же, как и условием растворения — его отвод в том же количестве.
В этом смысле и говорилось в комментарии, что «соль, смешиваясь с водой, «отдает свой долг» — то тепло, которое было затрачено на ее отделение от воды при добыче из раствора».
Заметим, что на «обратный эффект Крапивина»: пар, отводимый по трубке, все время имеет температуру 100'С, несмотря на то, что рассол нагрет до 110'С,— указал читатель А. Светиков (г. Северодонецк).
Может возникнуть вполне обоснованный вопрос: зачем заменять четкое объяснение разогрева на основе теплоты конденсации более сложным — за счет теплового эффекта растворения? Действительно, количественно через теплоту конденсации можно получить правильный результат '. Но качественно, с позиций второго начала термодинамики, тут возникают трудности. Почему, вопреки второму закону, тепло конденсации, выделяющееся при 100'С, передается «вверх» — более теплому рассолу. Нельзя же действительно удовлетвориться объяснением, что теплоте конденсации просто «некуда деваться».
Строго говоря, теплота смешения пара и рассола несколько меньше, чем теплота конденсации пара. Поэтому расчет по теплоте конденсации даст несколько завышенный результат, но этой разницей можно пренебречь.
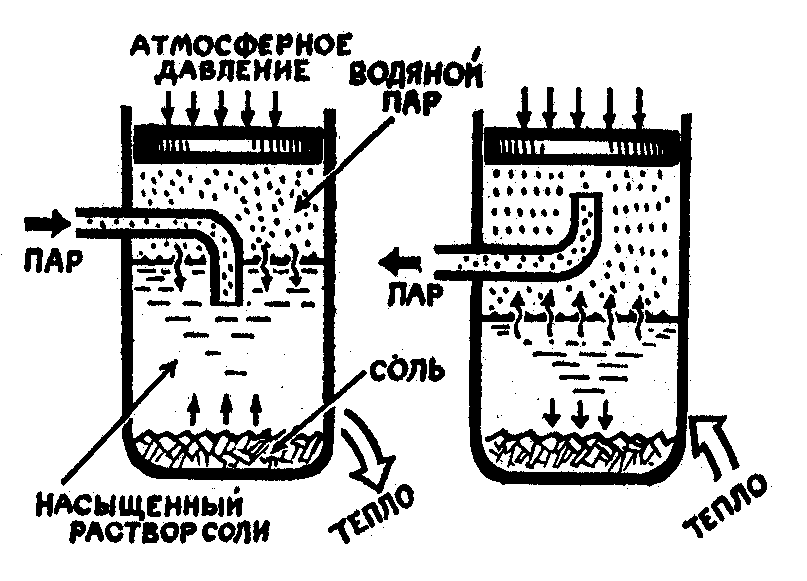
Рис. 1 Рис. 2.
Схемы видоизмененного опыта Крапивина.
Все дело в том, что в опыте Крапивина происходит сложный физико-химический процесс смешения, сопровождающийся переносом не только энергии, но одновременно и вещества. Если это учесть, то вообще снимается вопрос о передаче тепла. Нагрев происходит «внутри», в процессе самого смешения, как в любой экзотермической реакции: смесь «сама себя нагревает». Разделение происходящего в опыте Крапивина процесса на два самостоятельных физических эффекта — конденсацию и перенос тепла — это упрощение, которое и создает кажущееся противоречие со вторым началом, Чтобы внести ясность в суть обсуждаемого вопроса, очевидно, полезно напомнить высказывание самого профессора А. Шубникова о втором начале термодинамики: «...то, что оно утверждает, к сожалению, способен по-настоящему понять лишь весьма ограниченный круг лиц, если принять во внимание то невероятное количество ошибок, относящихся ко второму началу, которое можно найти не только в курсах физики, но и в курсах термодинамики. Описанное нами явление можно объяснить очень просто».
Из этого ясно, что профессор А. Шубников сознательно пошел на упрощение, стремясь к максимальной популяризации.
В действительности рассматриваемая в опыте Крапивина система состоит из трех сосуществующих фаз (жидкой, твердой, газообразной), компонентами которых служат вода и соль. Этот случай строго впервые подробно рассмотрен основоположником равновесной термодинамики сложных систем американским ученым Дж. У. Гиббсом в 1875 году. Он дал общий анализ таких систем, у которых число сосуществующих фаз на единицу больше числа независимых компонентов. Интересующихся этой проблемой отошлем к знаменитой работе Гиббса «О равновесии гетерогенных веществ» (в книге «Термодинамика. Статистическая механика». М., «Наука», 1982 г.), В более доступной форме идеи Гиббса изложил другой выдающийся ученый — Ван-Дер-Ваальс (см. «Курс термостатики», М., ОНТИ, 1936 г.).
Многие читатели справедливо указывают, что опыт Крапивина можно успешно провести и с водными растворами других солей. Разница только количественная: величины перегрева раствора в каждом случае будут свои.
С теоретических позиций представляет интерес письмо Ф. Руссу, который предлагает примирить «опыт Крапивина» и второе начало термодинамики весьма своеобразным путем.
Он пишет так: «В любом учебнике термодинамики можно найти следующее определение: системой называется тело или группа взаимодействующих между собой тел, изолированных от окружающей среды.
Уже это определение показывает, что профессор А. Шубников и доктор технических наук В. Бродянский допускают ошибку, когда в качестве системы рассматривают только пар и раствор. Колба с водой в процессе опыта непрерывно нагревается, поэтому пламя горелки также входит в состав системы. А в системе: пламя горелки, вода в колбе, пар и раствор ничего парадоксального не происходит. Теплота, как и полагается, переходит от более горячего тела — от пламени горелки, к более холодному — раствору. Пар служит лишь средством передачи тепла. Ясно, что никакое опровержение второго начала термодинамики не имеет места».
Чтобы установить, кто прав, а кто ошибается, нужно начать, очевидно, с уточнения понятия «система»; тогда станет ясным, что можно, рассматривать в качестве системы и как это делать.
Определение термина «система», которое дает Ф. Руссу, неправильно. Его нет ни в одном учебнике термодинамики.
Посмотрим в Сборник определений Комитета научно-технической терминологии Академии наук СССР. Там записано: «Термодинамическая система — тело (совокупность тел), способное (способных) обмениваться с другими телами (между собой) энергией и (или) веществом».
Никаких слов об обязательной изоляции от окружающей среды в общем определении термодинамической системы нет. Напротив, подчеркивается способность тел, составляющих систему, к обмену веществом и энергией. Конечно, может существовать и система, которая не в состоянии обмениваться через свои границы ни веществом, ни энергией,— изолированная система, но это лишь частный случай. Следовательно, в качестве рассматриваемой системы можно выбрать любое тело или совокупность тел. Поэтому никакой ошибки в том, что система ограничена только паром и раствором, нет. Ф. Руссу предлагает рассматривать более широкую систему, включив в нее и пламя горелки. Ход мысли здесь таков: «если в расширенной большой системе теплота «как и полагается» в конечном итоге переходит от более горячего тела (пламени горелки) к более холодному (раствору), то все в порядке, независимо от того, что происходит на промежуточных этапах».
Такое представление, на первый взгляд логичное, ошибочно в принципе. Если даже в самом малом участке системы второй закон не соблюдается, это означает его нарушение системой в целом, хотя внешне все выглядит благополучно. Следовательно, доказательство «переходом к большой системе» не имеет силы и от разбора взаимодействия пара и раствора уйти нельзя. Надо заниматься именно им.
Обзор писем читателей показывает, что научные вопросы, связанные с поведением и свойствами растворов твердых тел, жидкостей и газов, вызывают живой интерес.
Это и неудивительно: своеобразные явления в растворах не только создают парадоксы, но и широко используются в разных отраслях промышленности — химической, пищевой, нефтегазовой, металлургической... О том, что понимание законов, определяющих процессы в растворах, очень важно и для практики, хорошо написал читатель М. Галимов.
«Наше производство имеет прямое отношение к термодинамике. За годы работы на заводе приходилось немало ломать голову над многими, порой невероятными, загадками технологии. Представьте, отказывает в работе ректификационная колонна, казалось бы, безо всяких причин... Перебираешь десятки вариантов режима, перечитываешь еще и еще раз литературу... И вот загадка разгадана: находит она и теоретическое и практическое объяснение, и колонна, послушная твоей воле, начинает работать «как миленькая». Как приятно чувствовать радость одержанной победы! Очень интересная наша работа».
Доктор технических наук В. БРОДЯНСКИЙ.
...начало









